
資訊中心
作者:香雪生命科學(xué)
發(fā)布時(shí)間:2024-02-07
閱讀:5757
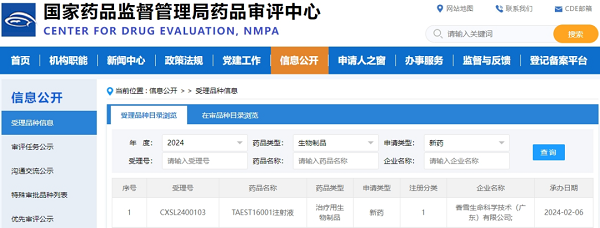
近日,香雪生命科學(xué)技術(shù)(廣東)有限公司 (簡(jiǎn)稱(chēng)“香雪生命科學(xué)”) 向國家藥品監督管理局提交了TAEST16001注射液新增適應癥臨床注冊申請并已獲得受理。TAEST16001注射液是中國首個(gè)獲得IND批件的TCR-T細胞免疫治療產(chǎn)品,首個(gè)臨床在研適應癥為晚期軟組織肉瘤,目前已經(jīng)進(jìn)入臨床II期,進(jìn)展順利。
關(guān)于TAEST16001
TAEST16001是香雪生命科學(xué)自主研發(fā)的TCR-T細胞免疫治療產(chǎn)品,針對NY-ESO-1癌胚抗原的TCR-T細胞,將病人的T細胞在體外用基因工程改造過(guò)的帶有腫瘤抗原特異性的TCR基因的慢病毒轉染,然后這些表達抗腫瘤抗原TCR的T細胞被大量擴增到約1×109~2×1010個(gè)細胞量,病人經(jīng)過(guò)適當劑量藥物進(jìn)行淋巴細胞清除(清淋)后,再把TCR-T細胞回輸給病人。
TAEST16001在研的首個(gè)適應癥為晚期軟組織肉瘤,以廣州中山大學(xué)腫瘤防治中心和北京大學(xué)腫瘤醫院作為牽頭單位,國內多家臨床機構正在參與II期臨床研究。
該產(chǎn)品首個(gè)I期臨床試驗為T(mén)AEST16001細胞在HLA-A*02:01陽(yáng)性并且表達NY-ESO-1抗原的晚期軟組織肉瘤患者中進(jìn)行的劑量遞增和拓展性研究。TAEST16001的I期臨床研究結果榮譽(yù)獲選美國臨床腫瘤學(xué)會(huì )(ASCO)2022年年會(huì )進(jìn)行口頭專(zhuān)題匯報,首次公開(kāi)臨床數據即獲得業(yè)界高度認可, 2023年國際著(zhù)名期刊Cell Reports Medicine發(fā)表該I期臨床研究文章,并邀請美國西北大學(xué)資深教授為文章作了特別點(diǎn)評,給予了高度評價(jià):“TAEST16001的I期臨床研究為過(guò)繼性T細胞免疫療法在晚期軟組織肉瘤的臨床轉化中邁出關(guān)鍵一步”。
關(guān)于香雪生命科學(xué)
香雪生命科學(xué)技術(shù)(廣東)有限公司(簡(jiǎn)稱(chēng)“香雪生命科學(xué)”)是一家聚焦TCR領(lǐng)域的細胞免疫治療產(chǎn)品和技術(shù)的研發(fā)企業(yè),是國內乃至國際上TCR-T細胞免疫治療頭部企業(yè)。
香雪生命科學(xué)有一支經(jīng)驗豐富,嚴謹扎實(shí)的研發(fā)團隊,基于自主知識產(chǎn)權的TCR核心技術(shù),已搭建完整的TCR-T產(chǎn)品研發(fā)技術(shù)體系和生產(chǎn)制備體系,其中TCR-T產(chǎn)品研發(fā)技術(shù)體系包含:①抗原肽發(fā)現平臺,②TCR高親和力平臺,③TCR-T開(kāi)發(fā)平臺;TCR-T生產(chǎn)制備體系包含:①自動(dòng)化細胞生產(chǎn)平臺,②質(zhì)控平臺;形成了TCR-T細胞產(chǎn)品全鏈條創(chuàng )新產(chǎn)業(yè)鏈。
香雪生命科學(xué)TCR-T產(chǎn)品布局廣泛,靶點(diǎn)豐富涉及包括CT抗原,新生抗原,病毒抗原等幾乎所有與腫瘤相關(guān)的特異性抗原,涵蓋A0201,A1101及A2402等多個(gè)以中國人群居多的HLA基因型,適應癥覆蓋多種臨床難治的實(shí)體瘤。
目前香雪生命科學(xué)已有兩個(gè)在研產(chǎn)品獲國家CDE批準進(jìn)入臨床,其中TAEST16001是中國首個(gè)獲得IND批件進(jìn)入臨床的TCR-T細胞治療產(chǎn)品;第二個(gè)產(chǎn)品是TAEST1901,在研的首個(gè)適應癥為原發(fā)性肝癌,正在啟動(dòng)I期臨床研究。