
資訊中心
作者:香雪生命科學(xué)研究中心--吳萬(wàn)里(翻譯轉載)
發(fā)布時(shí)間:2019-01-15
閱讀:12435
TCR表達在T細胞的表面,由兩條不同的蛋白鏈組成。在大多數成熟T細胞中,TCR由α和β鏈組成,在一小部分T細胞中,其TCR由γ和δ鏈組成。αβ-TCR的抗原識別在適應性免疫系統功能中占主導地位,αβ-TCR與抗原提呈細胞表面的“抗原肽-主要組織相容性復合物”(pMHC)結合。由于T細胞能夠區分外源性pMHC與自身pMHC,因此αβ-TCR與pMHC之間的相互作用具有高度的特異性。CD8+ T細胞在腫瘤患者的適應性免疫應答中起著(zhù)重要的作用,并通過(guò)TCR對特異性肽表位的識別而被激活,這些肽表位主要來(lái)源于內源性蛋白,由腫瘤細胞表面的MHCⅠ類(lèi)分子所遞呈。MHCⅠ類(lèi)分子是在幾乎所有有核細胞上表達的一種膜蛋白,它們由多個(gè)人類(lèi)白細胞抗原(HLA)的基因(HLA-A、B、C等)所編碼。HLA基因的表達可被干擾素(IFN)信號上調,但其在腫瘤中的表達往往被明顯地下調,下調程度與癌癥患者的免疫逃逸和疾病進(jìn)展相關(guān)。T細胞活化需要pMHC抗原與TCR的結合,然后進(jìn)入細胞內信號通路。體內外研究表明,遞呈抗原的數量決定了T細胞中細胞因子的表達情況。
Naive T細胞經(jīng)TCR/pMHC相互作用激活后,通過(guò)10~20輪的細胞分裂完成其克隆性擴增。相比于Naive T細胞,抗原刺激的T細胞通過(guò)一種叫做“功能性親和力成熟”的過(guò)程將其抗原應答性大大提高。研究發(fā)現,抗原刺激的T細胞比naive T細胞具有更強的增殖能力和細胞因子生成能力。T細胞通過(guò)TCR-CD3群簇識別抗原-MHC復合物,在MHC和TCR相互作用后,多種蛋白被激活了的受體招募至質(zhì)膜上并參與信號的傳導(圖2)。磷脂酶C-γ1(PLC-γ1)將膜磷脂酰肌醇二磷酸(PIP2)酶解成三磷酸肌醇(IP3)和二酰基甘油(DAG)。IP3與其內質(zhì)網(wǎng)上的受體相互作用上調胞漿中Ca2+水平,激活Ca2+結合的鈣調蛋白,隨后調節活化T細胞核因子(NFAT)蛋白。此外,DAG還激活RAS/胞外調節激酶(ERK)通路,調節核因子Fos。通過(guò)這些相互作用的信號通路,T細胞被激活,釋放出大量的細胞因子和趨化因子,包括γ-干擾素、顆粒酶B和IL-2。
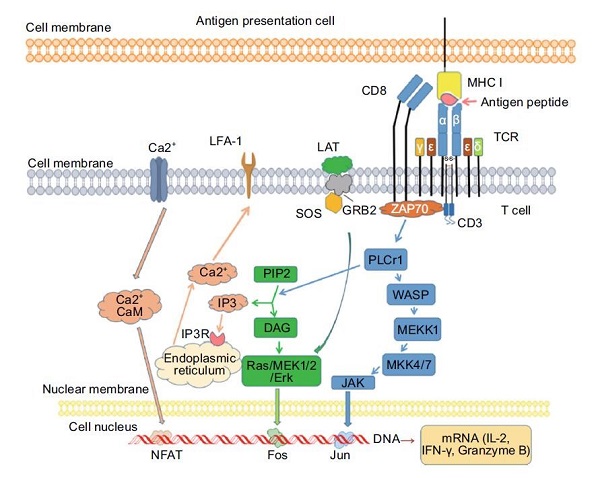
T淋巴細胞的功能主要受TCR信號的調控。研究表明,來(lái)自p38的初始TCR信號會(huì )相繼觸發(fā)維生素D受體(VDR)和PLC-γ1的誘導,這兩者都是經(jīng)典TCR信號傳導和T細胞活化所必需的。基因阻斷TCR的內化可以抑制T細胞的增殖,表明TCR信號是T細胞增殖所必需的。TCR的內化對于持續的信號傳遞和包括雷帕霉素靶標(mTOR)在內的關(guān)鍵代謝途徑的激活也是必需的。T細胞失能是一種免疫耐受機制,其作用是控制T細胞的活化,當淋巴細胞遇到抗原后其內在功能失活,這種現象在腫瘤微環(huán)境中經(jīng)常出現。通過(guò)“抗原誘導/腫瘤誘導失能模型"的研究發(fā)現,早期生長(cháng)反應蛋白2(Egr2)是體內失能誘導時(shí)所必需的。因此,Egr2被認為是T細胞失能的重要轉錄調節因子。T細胞的活化狀態(tài)和免疫應答水平進(jìn)一步受多種共刺激因子(CD 28、誘導T細胞共刺激因子ICOS和OX 40)和共抑制因子(細胞毒性T淋巴細胞相關(guān)抗原CTLA-4、程序性死亡蛋白PD-1)的控制。例如,在免疫檢查點(diǎn)PD-1缺失的情況下,融合抗體B7H1-Ig可以增強T細胞增殖和免疫應答。這表明,在基于B7H1介導的通路上干預、增強或下調免疫應答是可能的。
注:本文已獲得原文[1]作者(Ping Y)就原文翻譯以及網(wǎng)絡(luò )刊登的授權。 [1] Ping Y, Liu C, Zhang Y. T-cell receptor-engineered T cells for cancer treatment: current status and future directions [J]. Protein Cell, 2018,